
- •Системный подход в исследованиях жизнедеятельности человека
- •Механизмы организации живых систем
- •«Болезни цивилизации» и системный подход
- •Психогенные аспекты патологии и системный анализ
- •Реактивность
- •Специфический иммунный ответ
- •Строение иммунной системы
- •Клеточные основы иммунного ответа
- •Гуморальный иммунитет
- •Гипоксия
- •Изменения метаболизма при гипоксии
- •Нарушения работы систем организма
- •Морфологические проявления
- •Приспособительные реакции при гипоксии
- •Химические и лекарственные факторы
- •Избыточное питание
- •Физические факторы
- •Изменение атмосферного давления
- •Действие лучистой энергии
- •Повреждение клетки и межклеточных структур
- •Нарушения межклеточных взаимодействий
- •Повреждение клеточных органелл
- •Дистрофии
- •Белковая дистрофия
- •Гиалиновые изменения
- •Жировая дистрофия миокарда
- •Нарушение обмена нуклеопротеидов
- •Патология водно-электролитного обмена
- •Нефротические отёки
- •Кахексические отёки
- •Нефритические отёки
- •Почечные механизмы
- •Патофизиологические эффекты ацидозов и алкалозов
- •Показатели нарушения кислотно-основного состояния
- •Этиология и патогенез
- •Морфогенез
- •Макроскопические признаки
- •Микроскопические и ультраструктурные признаки
- •Клинико-морфологические формы
- •Апоптоз
- •Этиология и патогенез
- •Морфология
- •Сравнительная характеристика некроза и апоптоза
- •Биохимические отличия апопотоза от некроза
- •Нарушения регуляции апоптоза в патологии и его клиническое значение
- •Свободнорадикальная смерть клеток
- •Смерть клеток при действии ионизирующей радиации
- •Патогенез
- •Местное венозное полнокровие
- •Кровотечение
- •Внутренняя (кровяная) система коагуляции
- •Внешняя (тканевая) система коагуляции
- •Антикоагуляционная система крови
- •Фибринолиз
- •Эндотелий в коагуляции и фибринолизе
- •Тромбоциты
- •Тромбоз
- •Морфология тромба
- •Исходы тромба
- •Патогенез
- •Морфология двс-синдрома
- •Морфология ишемии
- •Инфаркт
- •Воспаление и иммунитет
- •Местные реакции при воспалении
- •Воспаление как общепатологический процесс
- •Гнойное воспаление
- •Продуктивное воспаление
- •Хроническое экссудативное воспаление
- •Воспаление вокруг паразитов и инородных тел
- •Патогенез
- •Стадии развития
- •Классификация
- •Изменения в органах и системах
- •Тепловой и солнечный удары
- •Гипотермия
- •Динамика заживления ран
- •Стадия резистентности
- •Стадия истощения
- •Механизм увеличения функционирующих структур
- •Механизм преобразования структур
- •Реакции гиперчувствительности типа II
- •Аутоиммунные болезни
- •Системные аутоиммунные заболевания
- •Органоспецифические аутоиммунные заболевания
- •Диссеминированные аутоиммунные заболевания
- •Иммунодефициты клеточного происхождения
- •Иммунодефициты гуморального происхождения
- •Амилоидоз
- •Эпидемиология опухолей
- •Этиология опухолей
- •Инфекционная теория канцерогенеза
- •Клеточные онкогены — промоторы опухолевого роста
- •Гены — супрессоры рака
- •Биохимический атипизм
- •Антигенный атипизм
- •Теории опухолевой трансформации
- •Предопухолевая дисплазия
- •Стадия инвазивной опухоли
- •Метастазирование
- •Строма опухоли
- •Ангиогенез в опухоли
- •Характер роста опухоли
- •Взаимодействие опухоли и организма
- •Классификация опухолей
- •Опухоли из эпителия
- •Нейроэндокринные опухоли
- •Опухоли мягких тканей
- •Опухоли меланинпродуцирующей ткани
- •Этиология
- •Диагноз
- •Расхождение диагнозов
- •Ятрогении
- •Патоморфоз
- •Дифференцировка клеток костного мозга
- •Патология эритроцитов
- •Эритроцитозы
- •Классификация анемий
- •Анемии при кровопотерях
- •Дисэритропоэтические анемии
- •Патология лейкоцитов
- •Лейкемоидные реакции
- •Гемобластозы
- •Новообразования миелоидной ткани
- •Острые миелоидные лейкозы
- •Миелодиспластические (миелопролиферативные) заболевания
- •Миелодиспластические синдромы
- •Новообразования лимфоидной ткани
- •Международная классификация новообразований лимфоидной ткани
- •III. Болезнь Ходжкина.
- •Острые лимфобластные лейкозы
- •Хронический лимфоцитарный лейкоз
- •Опухоли из плазматических клеток
- •Болезнь ходжкина
- •Лимфомы кожи
- •Опухоли из гистиоцитов
- •Опухоли из тучных клеток
- •Тромбоцитарные заболевания. Коагулопатии
- •Нарушения сосудистых факторов свёртывания
- •Нарушения плазменных факторов свёртывания
- •Гемофилия
- •Болезнь виллебранда
- •Нарушения тромбоцитарных факторов свёртывания
- •Атеросклероз
- •Гиперлипидемии
- •Патогенез атеросклероза
- •Основные этапы патогенеза атеросклероза
- •Доброкачественная гипертоническая болезнь
- •Заболевания сердца
- •Аритмии
- •Нарушения автоматизма
- •Нарушения проводимости
- •Нарушения возбудимости
- •Смешанные формы аритмий
- •Формы ибс
- •Инфаркт миокарда
- •Хроническая ишемическая болезнь сердца
- •Кардиомиопатии
- •Первичные кардиомиопатии
- •Вторичные кардиомиопатии
- •Миокардиты
- •Перикардиты
- •Сердечная недостаточность
- •Острая сердечная недостаточность
- •Хроническая сердечная недостаточность
- •Опухоли сердца
- •Приобретённые аневризмы артерий
- •Варикозное расширение вен
- •Обструкция лимфатических сосудов
- •Вторичные васкулиты
- •Сосудистые опухоли промежуточной группы
- •Строение и физиология лёгких
- •Нереспираторные функции лёгких
- •Механизмы защиты бронхолёгочной системы
- •Крупозная пневмония
- •Бронхопневмония
- •Отдельные виды острой интерстициальной пневмонии
- •Абсцесс лёгкого
- •Сосудистая патология лёгких
- •Хронические обструктивные заболевания лёгких
- •Хронический обструктивный бронхит
- •Бронхоэктатическая болезнь
- •Хроническая обструктивная эмфизема лёгких
- •Бронхиальная астма
- •Лёгочные васкулиты
- •Пневмокониозы
- •Дыхательная недостаточность
- •Рак лёгкого
- •Болезни плевры
- •Аномалии языка и слизистой оболочки рта
- •Аномалии слюнных желёз
- •Аномалии зубов
- •Кисты головы и шеи
- •Пульпит
- •Некариозные поражения твёрдых тканей зуба
- •Болезни пародонта
- •Гингивит
- •Пародонтит
- •Пародонтоз
- •Хейлиты
- •Глоссит
- •Язвенно-некротический гингивит
- •Кандидозный стоматит
- •Туберкулёз
- •Сифилис
- •Хронический сиаладенит
- •Сухой синдром Шёгрена
- •Опухоли слюнных желёз
- •Кисты челюстей
- •Опухолеподобные поражения челюстей
- •Мезенхимальные одонтогенные доброкачественные опухоли
- •Смешанные одонтогенные доброкачественные опухоли
- •Недостаточность пищеварения
- •Нарушения аппетита
- •Нарушение пищеварения в полости рта
- •Болезни пищевода
- •Дивертикулы пищевода
- •Хиатальная грыжа
- •Эзофагит
- •Врождённые и наследственные аномалии
- •Гастрит
- •Хронический гастрит
- •Опухоли желудка
- •Врождённые аномалии кишечника
- •Синдром мальабсорбции
- •Ишемическая болезнь кишечника
- •Аппендицит
- •Опухоли аппендикса
- •Колоректальный рак (рак толстой кишки)
- •Заболевания брюшины
Бронхиальная астма
Бронхиальная астма — хроническое рецидивирующее воспалительное заболевание. Характерна повышенная возбудимость трахеобронхиального дерева в ответ на различные стимулы, что приводит к пароксизмальному сужению воздухопроводящих путей.
Основные виды бронхиальной астмы: экзогенная (атопическая, аллергическая, реагин-обусловленная) и эндогенная (нереагиновая, идиопатическая, индуцированная различными факторами). Кроме того, бронхиальная астма может быть ятрогенной (лекарственной) и профессиональной.
● Экзогенная бронхиальная астма связана с аллергенами окружающей среды (частицы пыли, пыльца растений, пищевые факторы и др.). Нередка семейная предрасположенность. Патогенез связан с реакцией гиперчувствительности I типа, обусловленной иммуноглобулином E. Ранние изменения в бронхиальном дереве — результат связывания антигена тучными клетками, покрытыми IgE. Это приводит к высвобождению из них первичных медиаторов (лейкотриенов и др.), а затем вторичных (цитокинов, нейропептидов и др.). Медиаторы, выбрасываемые в острую фазу, вызывают бронхоспазм, отёк слизистой оболочки, секрецию слизи и инфильтрацию эозинофилами (рис. 11-8). Поздние изменения провоцируют лейкоциты инфильтрата (эозинофилы, нейтрофилы, моноциты). При этом наблюдают бронхоспазм, отёк, лейкоцитарную инфильтрацию и слущивание бронхиального эпителия.

Рис. 11-8. Взаимоотношения хронической обструктивной болезни лёгких с бронхиальной астмой.
● Эндогенная бронхиальная астма может быть связана с действием разных факторов (прежде всего, инфекционных, химических, лекарственных), однако точная причина гиперреактивности бронхов неизвестна. Семейный анамнез отсутствует в большинстве случаев. Изредка наблюдают реакцию гиперчувствительности, опосредованную IgE.
РЕСТРИКТИВНЫЕ ЗАБОЛЕВАНИЯ ЛЁГКИХ
Для рестриктивных заболеваний характерно уменьшение объёма лёгочной паренхимы и жизненной ёмкости лёгких. В эту группу входят интерстициальные болезни лёгких. В основе рестриктивных лёгочных заболеваний — развитие воспаления и фиброза в интерстиции респираторных отделов лёгких, нередко иммунной природы. Это ведёт к интерстициальному фиброзу, блокаде аэрогематического барьера и прогрессированию клинических симптомов дыхательной недостаточности. Большинство лёгочных заболеваний на поздних стадиях развития имеют одновременно обструктивные и рестриктивные нарушения.
Интерстициальные болезни лёгких — группа рестриктивных заболеваний с двусторонним, диссеминированным, острым или хроническим поражением интерстиция респираторных отделов, что приводит к интерстициальному фиброзу и снижению жизненной ёмкости лёгких.
История изучение интерстициальных болезней лёгких связана с именами американских врачей Хаммена и Рича, впервые описавших в 1935 г., а затем в 1944 г. в «Бюллетене госпиталя Джонса Гопкинса» особый вариант тяжёлого, быстропрогрессирующего поражения лёгких с интерстициальным фиброзом и тяжёлой дыхательной недостаточностью. Это заболевание они наблюдали у 6 больных и назвали острым диффузным интерстициальным фиброзом. Интерстициальные болезни лёгких имеют характерные клинические, рентгенологические и морфологические изменения, это позволяет объединять в одну группу более 100 заболеваний, различных по интенсивности поражения лёгких и прогнозу.
Морфология. Большинство интерстициальных болезней лёгких протекает с фиброзирующим альвеолитом. Это диффузное или очаговое, острое или хроническое негнойное воспаление интерстиция респираторных отделов (альвеол, альвеолярных ходов, бронхиол) с исходом в фиброз. Для обозначения фиброзирующего альвеолита употребляют множество терминов: склерозирующий альвеолит, идиопатический фиброзирующий альвеолит, диффузный интерстициальный фиброз, интерстициальный пневмонит, болезнь Хаммена–Рича, синдром Скеддинга, болезнь Ослера–Шарко, фиброзная дисплазия лёгких. Кроме того, перечисленными терминами часто называют патологический процесс, синдром и заболевание — идиопатический фиброзирующий альвеолит.
Фиброзирующий альвеолит — морфологическое проявление большинства интерстициальных болезней лёгких, в первую очередь, идиопатического фиброзирующего альвеолита, вторичных фиброзирующих альвеолитов при ревматических заболеваниях, аллергических экзогенных альвеолитах, пневмокониозах. Фиброзирующий альвеолит возникает не только при болезнях лёгких с диффузным поражением интерстиция, но и при гранулематозном воспалении. В последнем случае обнаруживают предгранулематозную стадию фиброзирующего альвеолита (пневмокониозы, саркоидоз).
Для всех интерстициальных болезней лёгких характерно развитие альвеолита в начале заболевания и интерстициального фиброза — в финале. Крайнее выражение интерстициального фиброза — сотовое лёгкое — сочетание интерстициального фиброза и кистозной трансформации терминальных и респираторных бронхиол. При этом возникают блокада аэрогематического барьера, вторичная лёгочная гипертензия, гипертрофия правого желудочка и лёгочное сердце. Особенности отдельных интерстициальных болезней выражены преимущественно на ранних стадиях их развития.
Этиология. Интерстициальные болезни лёгких могут быть вызваны вирусами, бактериями, грибами, действием органической и неорганической пыли, радионуклидов, гипероксией в условиях гипербарической оксигенации, токсическими факторами, лекарственными препаратами и др. Этиология большинства интерстициальных болезней лёгких, в том числе, идиопатического фиброзирующего альвеолита и синдрома Гудпасчера, неизвестна.
Среди лекарственных препаратов наиболее опасны цитостатики (блеомицин, бусульфан, кармустин, циклофосфамид, метотрексат, митомицин) и ряд других препаратов (амиодарон, амитриптилин, нитрофурантоин).
Пато- и морфогенез интерстициальных болезней лёгких зависит от характера первичного воспаления респираторных отделов. Важную роль в морфогенезе фиброзирующего альвеолита играют альвеолярные макрофаги и полиморфноядерные лейкоциты. В активированном состоянии эти клетки генерируют большое количество активных форм кислорода, протеаз и цитокинов, вызывающих одновременно повреждение и склероз лёгочной ткани. Повреждение альвеолярной перегородки может быть иммунным (при идиопатическом фиброзирующем альвеолите, саркоидозе) или неиммунным (при большинстве пневмокониозов). Повреждающий фактор может попадать с воздухом и поражать сначала эпителиальную выстилку альвеол, а затем лёгочный интерстиций. При иммунном процессе аспирированный инфекционный возбудитель или аллерген с диаметром частиц менее 1–3 мкм, антитела и сенсибилизированные T-лимфоциты также сначала повреждают капилляры, затем интерстиций и эпителий. Возможно сочетание описанных путей поражения.
Характерная черта интерстициальных заболеваний лёгких — развитие интерстициального фиброза как исход альвеолита. При этом важна репарация эпителия, зависящая от глубины повреждения.
● При интактной базальной мембране повреждение альвеолярного эпителия вызывает экссудацию в просвет альвеол, затем либо рассасывание экссудата, пролиферацию пневмоцитов II типа, восстановление структуры альвеол, либо организацию экссудата с образованием телец Массона (карнификацию).
● При разрушении базальной мембраны исход повреждения эпителия — фиброз и рубцевание. Альвеолярные макрофаги активируют синтез коллагена I типа и протеогликанов клетками лёгочного интерстиция — фибробластами и миофибробластами. Последние мигрируют в просвет альвеол, участвуя в образовании полей фиброза.
Классификация интерстициальных заболеваний лёгких. Выделяют заболевания с установленной и неустановленной (в большинстве случаев) этиологией, а по характеру продуктивного воспаления — интерстициальные и гранулематозные.
● Интерстициальные заболевания с установленной этиологией:
пневмокониозы, вызванные органической и неорганической пылью;
острые интерстициальные пневмонии (вирусные, грибковые, пневмоцистные, экзогенный аллергический альвеолит и др.).
● Интерстициальные заболевания с неустановленной этиологией:
идиопатический фиброзирующий альвеолит (болезнь Хаммена–Рича);
вторичный фиброзирующий альвеолит при ревматических болезнях, HBV-инфекции;
лёгочные васкулиты;
саркоидоз;
фиброзирующий альвеолит при синдроме Гудпасчера и других лёгочно-почечных синдромах;
идиопатический гемосидероз лёгких;
эозинофильная пневмония;
гистиоцитоз Х;
альвеолярный протеиноз;
десквамативная интерстициальная пневмония.
Особенности интерстициальных болезней лёгких связаны с рестриктивным характером изменений, резким снижением жизненной ёмкости лёгких и диффузионной способности кислорода, развитием одышки, тахипноэ, цианоза. Диагностика основана на клинико-лабораторных данных (симптом крепитации, рентгенологические признаки, исследование лаважной жидкости, открытая биопсия лёгкого). В лаважной жидкости выявляют увеличение количества нейтрофилов или лимфоцитов.
Идиопатический фиброзирующий альвеолит
Идиопатический фиброзирующий альвеолит — группа диффузных воспалительных заболеваний лёгких неустановленной этиологии с преобладанием диффузного острого или хронического поражения интерстиция респираторных отделов. При этом в интерстиции возникают воспаление и фиброз, приводящие к прогрессирующей лёгочно-сердечной недостаточности.
Для всех интерстициальных болезней лёгких характерно развитие альвеолита в начале заболевания и интерстициального фиброза — в финале. Крайнее выражение интерстициального фиброза — «сотовое лёгкое» — сочетание интерстициального фиброза и кистозной трансформации терминальных и респираторных бронхиол (рис. 11-9). При этом возникают блокада аэрогематического барьера, вторичная лёгочная гипертензия, гипертрофия правого желудочка и лёгочное сердце.
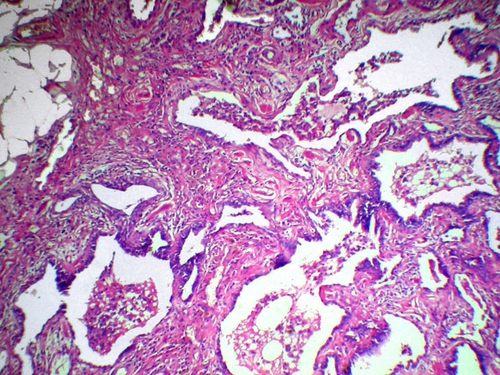
Рис. 11-9. Хроническая обычная интерстициальная пневмония, стадия сотового лёгкого. Окраска гематоксилином и эозином (x100).
Особенности интерстициальных болезней лёгких связаны с рестриктивным характером изменений, резким снижением жизненной ёмкости лёгких и диффузионной способности кислорода, развитием одышки, тахипноэ, цианоза.
В 1935 г. Хаммен и Рич описали быстро прогрессирующий диффузный лёгочный фиброз с непродуктивным кашлем, нарастающей одышкой, отёками, гипоксией мозга с эпизодами бреда и смертельным исходом уже через 4 мес после начала болезни. В интерстициальных структурах лёгких находили разрастание соединительной ткани. Стенки альвеол были значительно расширены, на ранних стадиях заполнены фибробластами, а на поздних — замещены зрелой рубцовой тканью. В отличие от пневмонии, альвеолы содержали очень мало воспалительного экссудата. Эти изменения в лёгких вызывали выраженные одышку и цианоз, а спустя несколько недель — дилатацию и гипертрофию правого желудочка с исходом в тяжёлую правожелудочковую недостаточность.
В нашей стране изменения в лёгких по типу синдрома Хаммена–Рича впервые описаны Е.М. Тареевым и В.А. Насоновой. Они наблюдали 5 больных ревматоидным артритом с поражениями лёгких и выделили сочетание своеобразно протекавшей интерстициальной пневмонии и гранулематоза.
Термин «фиброзирующий альвеолит» отражает основные признаки заболевания — воспаление и фиброз. В нашей стране наиболее употребителен термин «идиопатический фиброзирующий альвеолит», подчёркивающий первичность и неясную природу заболевания. В последнее время всё чаще используют понятие «обычная интерстициальная пневмония», отражающее наиболее частый морфологический субстрат заболевания. Сейчас идиопатический фиброз лёгких рассматривают отдельно от других идиопатических интерстициальных пневмоний.
Выделяют следующие виды идиопатического фиброзирующего альвеолита:
идиопатический фиброз лёгких, описанный впервые как синдром Хаммена–Рича, или криптогенный фиброз лёгких;
идиопатические интерстициальные пневмонии.
Термин «идиопатические интерстициальные пневмонии» противоречив. Назвав данную группу заболеваний пневмониями, необходимо обосновать их микробную этиологию, хотя термин «идиопатические» означает заболевания неустановленной этиологии. Группа идиопатического фиброза лёгких представлена идиопатическими хроническими и острыми пневмонитами (табл. 11-1). Перечисленные клинические формы заболевания и морфологические варианты не всегда совпадают.
Таблица 11-1. Соответствие морфологических вариантов и клинических форм идиопатического фиброзирующего альвеолита
Морфологические варианты |
Клинические формы |
Обычная интерстициальная пневмония |
Идиопатический фиброз лёгких |
Неспецифическая интерстициальная пневмония |
Неспецифическая интерстициальная пневмония |
Организующаяся пневмония |
Криптогенная организующаяся пневмония |
Диффузное поражение альвеол |
Острая интерстициальная пневмония |
Респираторный бронхиолит |
Респираторный бронхиолит с интерстициальной болезнью лёгких |
Десквамативная интерстициальная пневмония |
Десквамативная интерстициальная пневмония |
Лимфоцитарная интерстициальная пневмония |
Лимфоцитарная интерстициальная пневмония |
Подтверждением того, что идиопатический фиброзирующий альвеолит — не одно заболевание, а группа болезней служат не только морфологические, клинические и рентгенологические различия, но и различная реакция на противовоспалительную терапию, прогноз и продолжительность жизни пациентов.
Обычная интерстициальная пневмония
Обычная интерстициальная пневмония наиболее распространена среди идиопатических интерстициальных пневмоний. Характерно постепенное начало, затяжное течение, нарастающая одышка напряжения. У большинства пациентов бывают двусторонние нежные хрипы над базальными отделами лёгких, лихорадка, слабость, потеря веса. Рентгенологически типично двустороннее усиление лёгочного рисунка и симптом «матового стекла» в базальных отделах лёгких. В большинстве случаев уже при установлении диагноза обнаруживают изменения по типу «сотового лёгкого».
Морфология. В развитии фиброзирующего альвеолита выделяют начальную и позднюю стадии.
● Начальная стадия. Макроскопически лёгкие могут быть изменены незначительно, они неравномерно воздушны, полнокровны, с увеличенной плотностью. Микроскопические изменения характерны для экссудативного и экссудативно-продуктивного воспаления. Отличие идиопатического фиброзирующего альвеолита от других интерстициальных болезней лёгких — большая выраженность повреждения и склероза интерстиция респираторных отделов со скоплениями миофибробластов. При этом обнаруживают распространённые, мозаично расположенные фокусы поражения среди сохранной лёгочной паренхимы. Чем дольше длительность заболевания, тем больше площадь изменённой лёгочной ткани. В альвеолярных перегородках — явления отёка, воспалительная инфильтрация, начальные проявления склероза. Нарушение проницаемости сосудов приводит к скоплению экссудата в просветах альвеол, протеинозу, десквамации эпителия, выпадению фибрина вплоть до образования гиалиновых мембран. В экссудате обнаруживают большое количество альвеолярных макрофагов, лимфоцитов, полиморфноядерных лейкоцитов. Воспалительный инфильтрат в интерстиции представлен, в основном, лимфоцитами и макрофагами, нередко с примесью нейтрофилов. Последние находят, в основном, в просвете альвеол и лаважной жидкости.
Отличие обычной интерстициальной пневмонии — большое количество альвеолярных макрофагов моноцитоидного типа с усиленным синтезом белка. Об этом свидетельствует увеличение содержания в них белковых факторов, стимулирующих пролиферацию клеток — фибронектина, c-fos и c-sis онкопротеинов. Кроме того, в стадию начальных изменений при идиопатическом фиброзирующем альвеолите альвеолярные макрофаги интенсивно производят активные формы кислорода и ФНО-α. Поступая в лёгочную ткань, эти вещества могут сами оказывать повреждающее действие, в первую очередь, на альвеолярный и бронхиолярный эпителий. В лаважной жидкости — выраженный цитоз, чаще, чем при других интерстициальных болезнях лёгких преобладают нейтрофилы и лимфоциты.
● Поздняя стадия идиопатического фиброзирующего альвеолита. Макроскопически лёгочная ткань резиновой плотности, пониженной воздушности и эластичности. Характерно формирование ячеистых структур, напоминающих пчелиные соты — «сотовое лёгкое». Микроскопически выявляют выраженный склероз интерстиция респираторных отделов и кистозную перестройку лёгочной ткани. Паренхима лёгкого замещена грубой соединительной тканью, в неё замурованы кистозно-расширенные воздухоносные пространства — структуры «сотового лёгкого», выстланные изнутри аденоматозно-гиперплазированным альвеолярным эпителием. Происходит замещение пневмоцитов I типа гиперплазированными пневмоцитами II типа, нередко с признаками атипии, очаговой и атипической аденоматозной гиперплазии, а также очагами плоскоклеточной метаплазии и дисплазии эпителия. Аэрогематический барьер перестает функционировать из-за выраженного фиброза интерстиция альвеолярных перегородок и нарушения регенерации эпителиальной выстилки. Клиническое проявление этих нарушений — прогрессирующая дыхательная недостаточность.
◊ Лёгочный интерстиций расширен за счёт утолщения и редупликации эпителиальных и эндотелиальных базальных мембран. В нём происходит накопление всех типов коллагенов и резкое увеличение труднодеградируемых коллагенов IV и V типов. В зоне аэрогематического барьера — большое количество коллагеновых волокон, активированных фибробластов, фиброцитов, лимфоцитов, макрофагов. Активные фибробласты лёгочного интерстиция выявляют также в просветах альвеол и капилляров, что ведёт к запустеванию микрососудов и развитию не только блока аэрогематического барьера, но и гипертензии в малом круге кровообращения. Организация экссудата в просвете альвеол с последующей эпителизацией приводит к формированию телец Массона и карнификации.
◊ На поздних стадиях идиопатического фиброзирующего альвеолита происходит перестройка лёгочного эпителия. Альвеолоциты I типа на больших участках замещены альвеолоцитами II типа с незрелыми осмиофильными мультиламеллярными тельцами, нередко с признаками атипии. Нарушение синтеза сурфактанта и облитерация бронхиол способствуют развитию очагов ателектаза лёгочной ткани. Дисрегенераторные изменения лёгочного эпителия могут в дальнейшем привести к развитию рака лёгкого.
◊ В морфогенезе обычной интерстициальной пневмонии велико значение взаимодействия альвеолярных макрофагов, T-лимфоцитов, различных типов фибробластов, нейтрофилов, эозинофилов, альвеолярного и бронхиолярного эпителия.
◊ Активированные интерстициальные и альвеолярные макрофаги вместе с нейтрофилами и другими клетками воспалительного инфильтрата повреждают эпителий, выделяя активные формы кислорода, протеазы, ФНО-α. Эти клетки также активируют пролиферацию миофибробластов, ангиогенез и склеротические изменения, выделяя факторы роста. Интерстициальный фибробласт — основная эффекторная клетка в развитии склероза при идиопатическом фиброзирующем альвеолите. Интерстициальный склероз приводит к нарушению регенерации эпителия в респираторных отделах лёгкого и может способствовать развитию рака лёгкого.
Осложнения идиопатического фиброзирующего альвеолита: развитие лёгочного сердца и прогрессирование лёгочно-сердечной недостаточности.
Неспецифическая интерстициальная пневмония
Неспецифическая интерстициальная пневмония — одно из самых сложных для диагностики заболеваний, поскольку специфические признаки отсутствуют, а подобная морфологическая картина может иметь разнообразную этиологию. Среди клинических признаков преобладает медленно прогрессирующая дыхательная недостаточность. Рентгенологически определяют двустороннее сетчатое усиление лёгочного рисунка в базальных отделах, симптом «матового стекла».
Морфология. Преобладают воспалительные изменения в интерстиции альвеол (лимфогистиоцитарная инфильтрация), выраженные изменения микрососудов вплоть до фибриноидного некроза и развития деструктивно-продуктивных васкулитов. В отличие от обычной интерстициальной пневмонии миофибробластические фокусы отсутствуют. Процесс мозаичен, возможно чередование участков поражённой и относительно сохранной лёгочной ткани. Микроскопические изменения зависят от стадии процесса.
● Ранняя стадия. Типично воспаление с участием интерстициальных макрофагов и лимфоцитов, отёк стромы.
● Поздняя стадия. Формирование нерезко выраженного фиброза лёгочного интерстиция. Фиброзная ткань состоит только из грубоволокнистой соединительной ткани без очагов пролиферации фибробластов.
Для неспецифической интерстициальной пневмонии характерны относительно благоприятное течение, хороший эффект лечения глюкокортикоидами, высокая выживаемость.
Десквамативная интерстициальная пневмония
Десквамативная интерстициальная пневмония чаще возникает у лиц 40–45 лет. Характерно постепенное начало. В морфогенезе условно выделяют раннюю и позднюю стадии.
● Ранняя стадия. Типично накопление гиперактивных альвеолярных макрофагов в просветах альвеол, повреждение эпителия альвеол, гиперплазия и слущивание клеток эпителия в просветы альвеол.
● Поздняя стадия. Помимо альвеолярных макрофагов, в просвете альвеол присутствуют десквамированные клетки гиперплазированного альвеолярного эпителия с выраженной экспрессией ЕМА, панцитокератинов, ТФР-β, фактор роста фибробластов β и Кi67. Характерен выраженный склероз лёгочного интерстиция. По мере прогрессирования в просветах альвеол находят преимущественно пневмоциты II порядка. Часто наблюдают плоскоклеточную метаплазию альвеолярного эпителия. Вероятно, при десквамативной интерстициальной пневмонии, в отличие от обычной интерстициальной пневмонии, первично повреждение альвеолярного эпителия и вторичное вовлечение лёгочного интерстиция.
Для десквамативной интерстициальной пневмонии свойственно относительно благоприятное течение и прогноз, а также достаточно хороший эффект терапии глюкокортикоидами.
Организующаяся пневмония
Другое название — облитерирующий бронхиолит с организующейся пневмонией. Характерно подострое начало с выраженным сухим кашлем, у 60% больных — лихорадка. При рентгенографии лёгких видны очаговые, «пятнистые» затемнения, не исчезающие после приёма антибиотиков. Выделяют раннюю и позднюю стадии.
● Ранняя стадия. Характерно перибронхиолярное воспаление, интральвеолярный отёк, скопление экссудата в просветах бронхиол и альвеол, базальноклеточная гиперплазия бронхиолярного эпителия.
● Поздняя стадия. Отмечают перибронхиолярный склероз, карнификацию альвеол, атипическую базальноклеточную гиперплазию. Эпителиальные клетки в очагах атипической базальноклеточной гиперплазии активно экспрессируют TGF-β, фактор роста фибробластов β, цитокератины.
Острая интерстициальная пневмония
Острая интерстициальная пневмония (острое диффузное повреждение альвеол) впервые описана L. Hamman и A. Rich в 1935 г. (синдром Хаммена–Рича), как самостоятельная нозологическая форма выделена в 1986 г.
Морфологические изменения при острой интерстициальной пневмонии представлены диффузным альвеолярным повреждением, сходным с респираторным дистресс-синдромом взрослых. В раннюю и позднюю стадию микроскопические изменения различны.
● Ранняя стадия. Наблюдают сочетание интерстициального отёка паренхимы, экссудацию в просвет альвеол, формирование гиалиновых мембран, тромбоз капилляров.
● Поздняя стадия (обычно с третьей недели заболевания). Обнаруживают признаки интраальвеолярной и/или интерстициальной организации, обычно с пролиферацией альвеолоцитов II типа.
Характерно фульминантное течение и плохой прогноз (летальность до 70%).
Респираторный бронхиолит
Респираторный бронхиолит с интерстициальной болезнью лёгких — самостоятельная форма идиопатического фиброзирующего альвеолита с развитием хронического бронхиолита. Обычно данное заболевание обнаруживают у курильщиков.
Характерно наличие интерстициального воспаления и фиброза средней степени выраженности в сочетании с хроническим бронхиолитом. Видны дисрегенераторные изменения эпителия в виде слизистой гиперплазии, плоскоклеточной метаплазии и дисплазии, наличие в просвете респираторных бронхиол и альвеол макрофагов с гранулами пигмента в цитоплазме. Респираторный бронхиолит — наименее изученная форма идиопатического фиброзирующего альвеолита.
Криптогенная организующаяся пневмония
Криптогенная организующаяся пневмония — заболевание неустановленной этиологии с клиническими и рентгенологическими признаками пневмонии. Синонимы: облитерирующий бронхиолит с организующейся пневмонией, облитерирующий бронхиолит, организующиеся пневмониоподобные фокусы, неразрешившаяся хроническая пневмония.
Морфологически для криптогенной организующейся пневмонии, в отличие от других форм идиопатического фиброзирующего альвеолита, характерны очаги карнификации в дистальных участках респираторного тракта, захватывающих бронхиолы, альвеолярные ходы и альвеолы, очаговость и однообразие поражений, сохранение архитектоники лёгкого и хроническое умеренно выраженное интерстициальное воспаление.
Экзогенные аллергические альвеолиты
Экзогенные аллергические альвеолиты (пневмониты гиперчувствительности) — группа острых и хронических интерстициальных заболеваний, вызванных вдыхаемыми аллергенами. Нередко аллерген бывает неустановлен. Наиболее частые вдыхаемые аллергены — термофильные актиномицеты, плесени, антигены животного происхождения. Выделяют профессиональные и бытовые альвеолиты, вызываемые вдыханием аллергенов.
● Профессиональные аллергические альвеолиты:
лёгкое фермера (плесени сена — Mycropolyspora faeni);
багассоз (плесени сахарного тростника — Thermoactinomyces sacchari);
сиквоз (плесени древесной пыли);
лёгкое заготовителей коры клена (Cryptostroma corticale);
лёгкое бондаря;
лёгкое заготовителей грибов.
● Бытовые аллергические альвеолиты:
лёгкое, вызванное увлажнением воздуха (плесени в кондиционерах, бассейнах, батареях центрального отопления);
болезнь любителя птиц (помет, кровь птиц);
лёгкое нюхателя табака.
Патогенез гиперергических альвеолитов до конца не изучен. С одной стороны, механизм развития заболевания связан с реакцией гиперчувствительности — иммунокомплексной и T-цитотоксической (III и IV типов) к вдыхаемым аллергенам. В сыворотке крови пациентов можно обнаружить антитела класса IgG к соответствующим аллергенам. С другой стороны, не все лица, имеющие антитела IgG к этим аллергенам, страдают гиперергическими пневмонитами. Это указывает на возможную генетическую предрасположенность к развитию заболевания.
Морфология экзогенных аллергических альвеолитов включает структурные изменения, отражающие путь проникновения аллергена в респираторные отделы лёгкого (наличие диссеминированных очагов вокруг респираторных бронхиол — бронхиолит в сочетании с интерстициальной пневмонией). Иммунное воспаление на основе реакций гиперчувствительности нередко вызывает образование неказеозных гранулём. Для острого течения характерно наличие альвеолита с преобладанием нейтрофилов, а для хронического — выраженный интерстициальный фиброз вплоть до развития «сотового лёгкого». Основные морфологические проявления:
инфильтрация лимфоцитами и макрофагами с примесью плазмоцитов (лимфоцитарный альвеолит);
в инфильтрате возможно наличие эозинофилов, при остром процессе — нейтрофилов;
гранулёмы в интерстиции без фокусов казеозного некроза;
интерстициальный фиброз вплоть до развития очагов карнификации и «сотового лёгкого», трудно отличимые от обычной интерстициальной пневмонии.
Клиническая характеристика острых и хронических экзогенных аллергических альвеолитов различна.
● Острый альвеолит возникает под действием высоких концентраций антигена. Тяжёлая одышка, кашель, лихорадка и озноб возникают уже через 4–6 ч после контакта. Выздоровление обычно наступает через несколько дней. При повторном контакте с аллергеном возможен рецидив.
● Хронический альвеолит возникает при длительном контакте с низкими концентрациями антигена. Характерно медленное нарастание одышки, кашля, общей слабости.
Для диагностики гиперергических пневмонитов используют кожные пробы и определение антител в крови. В трудных случаях проводят биопсию лёгкого. Принципы лечения экзогенных аллергических альвеолитов: устранение контакта с антигеном и назначение глюкокортикоидов, особенно в острую стадию.
Идиопатические интерстициальные заболевания с гранулёматозом лёгких
Саркоидоз
Саркоидоз — системное заболевание неустановленной этиологии с развитием неказеозных гранулём (макрофагальных, эпителиоидноклеточных, гигантоклеточных) в лёгких, лимфатических узлах и других органах. Диагноз саркоидоза ставят на основании клинико-лабораторного и рентгенологического подтверждения поражения более чем одного органа, если в них морфологически выявлены неказеозные гранулёмы, а также исключены другие причины развития гранулём саркоидного типа.
Саркоидоз — наиболее частое заболевание среди интерстициальных болезней лёгких с неустановленной этиологией, распространён повсеместно, у лиц любого возраста. Пик заболеваемости — возраст 20–40 лет. Заболеваемость саркоидозом выше среди женщин. В отдельных расовых и этнических группах саркоидоз диагностируют чаще, что говорит о наличии генетической предрасположенности. Так, в Северной Америке заболеваемость саркоидозом среди чернокожего населения в 15 раз выше, чем среди белого. Чрезвычайно высока заболеваемость саркоидозом среди женщин Ирландии, а также скандинавских стран (200 и 64 на 100 тыс. соответственно). Заболевание может протекать бессимптомно и быть обнаружено случайно рентгенологически или при аутопсии.
Этиология саркоидоза неизвестна. Предполагают участие в развитии саркоидоза L-форм Mycobacterium tuberculosis, Borrelia burgdorferi, Propionibacterium acnes, микоплазм, хламидий и вирусов. Возможную роль микобактерии туберкулёза подтверждает обнаружение у больных саркоидозом изменений, типичных для туберкулёза: положительные данные ПЦР на фрагменты ДНК микобактерий в саркоидных гранулёмах, наличие γ-δ-T-клеток, ассоциированных с микобактериальными инфекциями.
Патогенез саркоидоза — иммунный с развитием реакции гиперчувствительности IV типа с избыточным количеством CD4+ T-лимфоцитов. У пациентов обнаруживают изменение кожных реакций ГЗТ, появление циркулирующих иммунных комплексов, признаки активации B-клеток. Резкое увеличение количества CD4+ T-лимфоцитов изменяет соотношение CD4+/CD8+, составляющее 1:10 (в норме 1:2). Причины пролиферации и накопления CD4+ T-лимфоцитов пока не установлены. CD4+ T-лимфоциты синтезируют цитокины, в том числе, γ-интерферон. Он вызывает трансформацию макрофагов в эпителиоидные, а затем гигантские многоядерные клетки с образованием неказеозных гранулём. Иммунный патогенез саркоидоза подтверждают следующие признаки:
лимфоцитарный характер альвеолита с накоплением CD4+ T-лимфоцитов, усиленно синтезирующих γ-ИФ, ИЛ-2 и вызывающих экспрессию HLA-DR;
активация альвеолярных макрофагов, выделяющих ИЛ-1, 12, 15, а также ФНО-α, факторы роста и свободные радикалы кислорода;
снижение количества циркулирующих T-лимфоцитов при нормальном уровне B-лимфоцитов;
неспецифическая поликлональная стимуляция B-лимфоцитов с развитием гипергаммаглобулинемии.
По характеру течения саркоидоз может быть острым или хроническим.
● Острый саркоидоз. Возникает острое поражение лёгких, других органов и лимфаденопатия. Синдром Лефгрена (особый вариант острого саркоидоза с развитием узелковой эритемы, двусторонней лимфаденопатии грудных узлов и полиарталгии) диагностируют у 20–50% пациентов. Для этого варианта характерны хороший прогноз и возможность спонтанной ремиссии в течение 2 лет.
● Хронический саркоидоз. Типично скрытое начало и постепенное прогрессирование заболевания с возможными спонтанными ремиссиями. Гистологическое исследование подтверждает наличие в органах и тканях саркоидных гранулём (рис. 11-10), иммунного воспаления с лимфогистиоцитарной инфильтрацией, васкулитов (в 2/3 случаев).
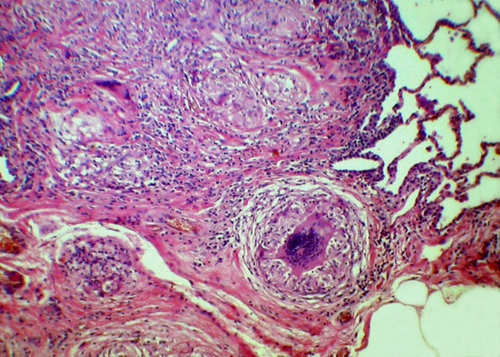
Рис. 11-10. Саркоидоз лёгкого. Окраска гематоксилином и эозином (x100).
Лёгкие при саркоидозе поражены в 90–95% случаев. Изменения в лёгких протекают в две стадии.
● Стадия лимфоцитарного альвеолита. Минимально выражены признаки воспаления со слабой лимфогистиоцитарной инфильтрацией, отсутствием характерных гранулём (догранулематозная стадия).
● Стадия гранулематозного воспаления. Морфологические особенности саркоидных гранулём:
отсутствие казеозного некроза;
«штампованный» вид за счёт расположенных на периферии фибробластов и коллагена;
единообразная морфология (одинаковая стадия гранулём).
Изредка при саркоидозе в гранулёмах находят мелкие очаги некроза, что затрудняет их дифференциальную диагностику с туберкулёзными гранулёмами.
Саркоидные гранулёмы — типичные гранулёмы иммунного типа. Они состоят из клеток моноцитарного происхождения — макрофагов, эпителиоидных и гигантских многоядерных клеток типа Пирогова–Лангханса, CD4+ T-лимфоцитов и фибробластов. Примерно в 60% случаев в гигантских многоядерных клетках можно обнаружить характерные цитоплазматические включения — звёздчатые, или астероидные тельца, имеющие вид звёздчатых кристаллов. Кроме того, в ткани лёгкого выявляют кальцифицированные пластинчатые тельца Шаумана, содержащие соли кальция и железа, а также тельца Хамазаки–Весеберга жёлто-коричневого цвета со свойствами липофусцина.
Поражение бронхов при саркоидозе может протекать с развитием эндобронхита и поражением слизистой оболочки бронхов вплоть до обструкции их просветов гранулематозной тканью. Сосудистую патологию лёгких при саркоидозе выявляют у 2/3 пациентов. Характерно развитие васкулитов с поражением ветвей лёгочной артерии и вен. Васкулиты имеют обычно гранулематозный характер, однако описаны продуктивные васкулиты с лимфоплазмоклеточной инфильтрацией. В результате могут возникать лёгочная гипертензия и лёгочное сердце, а также окклюзия вен.
Клинические признаки разнообразны, они зависят от поражения органов и активности процесса. Часто заболевание протекает бессимптомно. Возможны лихорадка, повышенная потливость ночью, узловая эритема, полиартрит. В сыворотке крови повышен уровень IgG, усилена активность ангиотензинконвертазы, а в моче — выделение кальция. Рентгенологические признаки: двусторонние интерстициальные инфильтраты и лимфаденопатия. Окончательный диагноз обычно ставят на основании биопсии.
Осложнения и исходы саркоидоза. В большинстве случаев прогноз хороший. Возможно спонтанное излечение, после него 65–70% пациентов имеют минимальные остаточные изменения, связанные с незначительным пневмосклерозом. У 20% пациентов саркоидоз протекает как медленно прогрессирующее хроническое заболевание с эпизодами обострений и ремиссий. В 10% случаев саркоидоз приводит к прогрессирующему фиброзу лёгких с развитием лёгочного сердца и лёгочно-сердечной недостаточности. Описаны единичные случаи развития аспергиллёза с формированием каверн и кровохарканием.
Некротизирующий саркоидный гранулематоз
Некротизирующий саркоидный гранулематоз описан впервые Либовым в 1976 г. Характерно сочетание сливных саркоидных и эпителиоидноклеточных гранулём с гранулематозным васкулитом и крупными полями некроза.
Этиология заболевания не установлена. Случаи некротизирующего саркоидного гранулематоза с васкулитами наблюдают при хронической инфекции, вызванной вирусом гепатита B. О возможной роли вирусной инфекции говорит выявление вирусных антигенов в лаважной жидкости пациентов.
Патогенез иммунный, он основан на развитии реакций гиперчувствительности III и IV типа в ответ на неизвестный антиген. Наличие иммунокомплексных реакций косвенно подтверждает развитие васкулита при данном заболевании.
Морфология некротизирующего саркоидного гранулематоза отличается от морфологии саркоидоза. При данном заболевании характерно гранулематозное поражение исключительно лёгких без вовлечения бронхопульмональных и других лимфоузлов. Гранулёмы также отличаются от саркоидных наличием в них некроза, а также расположением гранулём вокруг некротизированных тканей. Васкулиты с поражением артерий и вен могут быть как гранулематозными с некрозом и без него, гигантоклеточными и деструктивно-продуктивными с фибриноидным некрозом и лимфогистиоцитарной инфильтрацией.
