
- •1. Элементы подгр. 1а. Строение атомов, сравнение свойств атомов, распространение в природе. Получение простых веществ и их свойства.
- •2.Элементы подгр. 2а. Строение атомов, сравнение свойств атомов, распространение в природе. Получение простых веществ и их свойства.
- •3. Оксиды и гидроксиды металлов ia групы
- •4)Оксиды и гидроксиды элементов 2а. Свойства, получение Соединения металлов главной подгруппы II группы Оксиды металлов iiа группы
- •Гидроксиды металлов iiа группы
- •6)Оксид и гидроксид алюминия. Получение и свойства
- •7.Амфотерность оксида и гидроксида алюминия. Комплексные соединения алюминия.
- •8. Бериллий. Получение и свойства
- •Получение:
- •Химические свойства:
- •Производство и применение:
- •Легирование сплавов
- •9. Цинк. Получение и свойства.
- •11.Медь получение и свойства
- •12.Соединение меди(1) и меди(2),их кислотно-основные и окислительно-восстановительные свойства. Комплексные образования.
- •13. Серебро, химические св-ва.
- •15)Положение в периодической системе
- •Строение атома
- •19. Марганец, получение, химические свойства.
- •23. Кадмий и его соединения.
1. Элементы подгр. 1а. Строение атомов, сравнение свойств атомов, распространение в природе. Получение простых веществ и их свойства.
В 1А подгр. входят Li(литий), Na(натрий), К(калий), Rb(рубидий), Cs(цезий), Fr(франций)
Это щелоч. Me, тк при взаим. с H2O обр. едкие щелочи
Fr-радиоактивный эл-т, поэтому его св-ва изучены мало
Атомы
этих эл-тов имеют на внешн. энергетич.
уровне 1 s-электрон.

Вступая в хим. взаим., атомы легко отдают электрон внешн. энерг. ур-ня, проявляя постоянную степень окисл +1
Поэтому они сильные восстанов.
По группе ↓ увелич. радиусы атомов, тк увелич. число электр. слоев. Уменьш. энергия ионизации (кол-во энергии, кот. требуется для того чтобы оторвать электрон от свободного атома. След. увелич. восстанов. и металл-ие св-ва.
Li+ образует кристаллогидраты. Поляризующая способность велика (смещение электр. плотности иона под действием электр. поля
Na+ половина соед-ий обр-ют кристаллогидраты. Увелич. радиуса уменьш. поляризующую способность
K+ Rb+ Cs+ комплексов не обр., след их соли не явл. кристаллогидратами
По многим химическим свойствам несколько отличается от других щелочных металлов Li+, имеющий диагональное сходство с Mg2+
Распр. в природе:
Na, K - 2%
Li
-
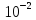 %
%
Rb,
Cs
-
 %
%
Rb, Cs рассеянные эл-ты, не обр собств. минералов, сопутствуют минералам Na, K
Минералы Li:
Li2O • Al2O3 • 4SiO2 – сподумен
Na:
NaCl – поваренная соль
Na2SO4 • 10H2O – глауберова соль
NaNO3 – чилийская селитра
Na3AlF6 - криолит
Na2B4O7· 10H2O - бура
Ka:
KCl • NaCl – сильвинит
KCl • MgCl2 • 6H2O – карналлит
K2O • Al2O3 • 6SiO2 – полевой шпат (ортоклаз)
Физ. св-ва
Низкие темпер. плавл. (30-180⁰):( Cs-28.5 Li - 180.5) , малые знач. плотн., мягкие, режутся ножом, проводят эл. ток. Серебристо-белые. Легкоплавкие.
Прим-ние
Li: явл. Me оборонной промышл. Примен. в виде сплавов с Mg в произв. водородных бомб, в состав смазочных масел, аккумуляторов, стекла. Токсичен. Li2СO3 исп. для лечения маниакально-депрессивного психоза. Повышенное содерж. Li в крови явл признаком нарушения ф-ции почек
Na: использ. в промышл. в теплообменниках ядерных реакторов. В организме чел. содерж. 100 г. 30% в костях. Явл. межклеточным катионом, регулирующим гомеостаз
К: исп. в производстве удобрений, в хим промышл, для варки стекла. В организме 140 г. 98% внутри клеток. Необходим для поддержания нервно-мышечной возбедимости, внутриклеточного осмотического давления, обеспечивает сокращение мышц, проницаемость мембран
Rb, Cs: в организме в очень малых кол-вах. По св-вам в орган. схожи с К
Получение:
*электролиз расплавов NaOh (небольшие энергозатраты, но О2 выделяющийся окисляет Na)
K (-): Na+ +1e =Na
A (+): 4OH− −4e =2H2O + O2
*электролиз расплава NaCl (высокая темп. плавл - 800)
K (катод) (-): Na+ + 1e = Na
A (анод) (+): Cl− — 2e = Cl2 *эвтектический сплав - NacK. натрий отделяют путем вакуумной перегонки от калия. Потом сублимируется
Хим. св-ва
*+H2 = гидраты (белые кристаллические порошки)
2Li+h2=2LiH (небольш. темп)
(остальные при высоких темп)
*+ галогены. р-ция активная с воспламенением
2Na+Br2=2NaBr
*2 Na + S = Na2S (совзрывом)
*6Li + N2 = 2Li3N (литий при комнатн. темп, остальные при высоких - 2000)
*2Li + 2C =2Li2C2 (карбиды) (1000)
* + вода
2Na + 2H2O = 2NaOH + H2(может загореться)
2Li + 2H2O = 2LiOH + H2(спокойно, не загораясь)
2K+H2O=2KOH + H2 (возгорание)
*+кислород (при комннат. темп)
4Li + O2 → 2Li2O(оксид лития)
2Na + O2 → Na2O2 (пероксид натрия)
K + O2 → KO2 (надпероксид калия)
На воздухе щелочные металлы мгновенно окисляются. Поэтому их хранят под слоем органических растворителей (керосин и др.).
*+ кислоты
Щелоч. ме взаим. с хлороводородной и разб. серной кислотами с выдел. водорода:
2Na + 2HCl = 2NaCl +H2
Конц. серную кислоту восстанавливают главным образом до сероводорода:
8Na + 5H2SO4 = 4Na2SO4 + H2S + 4H2O
с разб. азотной кислотой получается аммиак или нитрат аммония, а с конц. – азот или оксид азота (I):
8Na +10HNO3(разб.)= 8NaNO3 + NH4NO3 + 3 H2O
8K +10HNO3(конц.)= 8KNO3 + NO2 + 5H2O
* окрашивание пламени
Li+ – карминово-красный
Na+ – желтый
K+, Rb+ и Cs+ – фиолетовый
