
ФХ 3 курс экзамен. Теория и препараты
.pdf
Запах аммиака в результате разложения мочевины и фиолетовый цвет при биуретовой реакции.
Количественный анализ
См Н2О2
Хранение
Хранят ЛС водорода пероксида в прохладном, защищенном от света, месте. Концентрированный раствор водорода пероксида взрывоопасен
Применение
Антисептическое по аналогии с перекисью. Наружно после растворения в воде
Препарат
натрия тиосульфат Natrii thiosulfas Na2S2O3*5H2O
Физические свойства
Бесцветные прозрачные кристаллы
Подлинность
С нитратом серебра дает белый осадок который желтеет

Схлоридом железа 3 образуется фиолетовый осадок тиосульфата железа
Ссоляной кислотой опалисценция и запах серы
Количественный анализ
Йодометрическое титрование с крахмалом. Обесцвечивание синей окраска в ТЭ
Хранение
Хранят в укупоренной таре из оранжевого стекла (тк S выпадает).
Применение
При отравлениях . При отравлении солями тяжелых металлов (ртути, мышьяка, таллия, свинца) переводит их в малорастворимые комплексные тиосульфаты. Цианиды превращает в тиоцианаты.
Препараты-соединения VII группы
Препарат
Натрия хлорид Natrii chloridum NaCl калия хлорид Kalii chloridum KCl
натрия бромид Natrii bromidum NaBr калия бромид Kalii bromidum KBr
натрия йодид Natrii iodidum NaI калия йодид Kalii iodidum KI
Физические свойства
Бесцветные кристаллы или белый кристаллический порошок без запаха, гигроскопичен
Подлинность
Качественные на катионы:
Na+
1)Желтое пламя
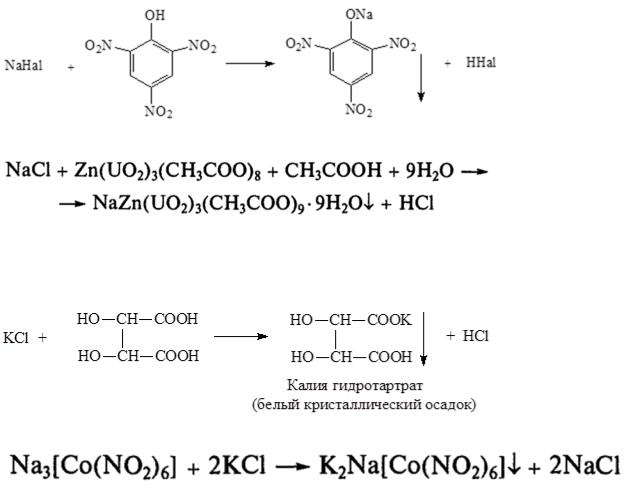
2)С пикриновой кислотой желтый осадок
3)С цинкуранилацетатом зелено-желтый комплексный осадок
K+
1)Фиолетовое пламя
2)С винной кислотой белый осадок
3)С гексацианокобальтатом натрия осадок желтого комплекса
На анионы
1) С AgNO3 осадки

2)Вытеснительный ряд галогенов
3)Йодиды с ацетатом свинца образуют золотисто-желтые чешуйки
4)Йодиды с ртутью оранжево-красный осадок
Количественный анализ
Аргентметрия
Р-я индикации
Изб
Ост
Р-я индикации
Р-я индикации
Метод Мора: индикатор хромат калия. Исп для Cl и Br
Метод Фаянса : адсорбционные индикаторы (эозинат Na). Исп для I
Метод Фольгарда : избыток титранта оттитровывают тиоцианатом аммония. Индикатор железоамонийные квасцы. Исп для Cl Br I
Хранение
Cl в укупоренной таре. Br I в укупоренной таре из оранжевого стекла от света

Применение
NaCl изотонический плазмозамещающий раствор (физ. раствор) при кровотечениях и отравлениях. Гипертонический р-р (10%) наружно при лечении гнойных ран.
KCl при гипокалиемии
NaBr, KBr угнетает ЦНС т.е. седативное действие при гипервозбудимости и бессоннице
NaI KI при гипертиреозе, для профилактики радиоактивного поражения щитовидной железы
Препарат
натрия фторид Natrii fluoridum NaF
Физические свойства
Бесцветные кристаллы или белый кристаллический порошок; растворим в воде.
Подлинность
Ализариновый комплекс циркония со фторид ионами в кислой среде меняет цвет раствора с красно-фиолетового на желтый
С Ca2+ и Ba2+ белый осадок
Тиоцианат железа (III) разрушается фторид-ионами с образованием бесцветных фторидных комплексов железа (III)

Количественный анализ
Кислотно-основное титрование в неводной среде.
Кипятят в уксусном ангидриде и ацетат натрия титруют хлорной кислотой. Индикатор фиолетовый кристаллический
Хранение
Хранят в укупоренной таре из оранжевого стекла
Применение
В зубных пастах для защиты эмали
Препарат
кислота хлороводородная 25% Acidum hydroghloridum HCl
Кислота хлороводородная разведенная 8% Acidum hydrochloridum dilutum HCl
Физические свойства
Бесцветный прозрачный раствор с острым запахом хлористого водорода
Подлинность
Индикаторы на кислою среду (метиловый оранжевый) дающий красный цвет
Восстановление хлора сильными окислителями (KMnO4, K2Cr2O7)
Количественный анализ
Прямая алкалиметрия. Обесцвечивание метиленового оранжевого
HCl + NaOH → NaCl + H2O

Аргентометрия для хлора (метод Мора или Фольгарда)
Хранение
В укупоренной таре
Применение
При пониженной кислотности желудочного сока
Препарат
раствор йода спиртовой 5% Iodi solution spirituosa I2 + KI
Физические свойства
Бурая жидкость и характерным запахом
Подлинность
Цвет в кислородосодержащих растворителях (вода спирт) бурый, в бескрислородных (хлороформ) фиолетовый.
Синяя окраска с крахмалом
Количественный анализ
Йодомерическое титрование с крахмалом до обесцвечивания раствора

KI определяют аргентометрией по Фаянсу (эозинат) в этой же обесцвеченной аликвоте. Тк реакцию дают NaI и KI поэтому объем серебра нитрата, пошедшего на титрование непосредственно калия йодида, определяют по разности между общим объемом серебра нитрата, пошедшего на титрование суммы йодидов, и объемом стандартного раствора натрия тиосульфата, пошедшего на определение йода
Хранение
В склянках с притертой крышкой из оранжевого стекла. В сухом прохладном месте.
Применение
5% Наружно как антисептик 1% (р-р Люголя) смазывание небных миндалин при ангинах.
Препараты-соединения III, IV, V групп
Препарат
Кислота борная, Acidum boricum H3BO3 B(OH)3 натрия тетраборат Natrii tetraboras Na2B4O7 · 10H2O
Физические свойства
H3BO3 Бесцветные, блестящие, жирные на ощупь чешуйки без запаха.

Na2B4O7 Бесцветные, прозрачные, легко выветривающиеся кристаллы или белый кристаллический порошок
Подлинность
H3BO3
Борноэтиловый эфир горит зеленым цветом
Реакция с куркумином. Образует комплексное соединение — розоцианин (розовый цвет)
Na2B4O7
Образование борной кислоты и ее проверка
Определение реакции среды в комплекса глицерина и тетрабората (кислая)
Количественный анализ
H3BO3 Ацидиметрия комплекса борной кислоты с глицерином который имеет более кислую среду чем просто борная кислота. Индикатор ф-ф
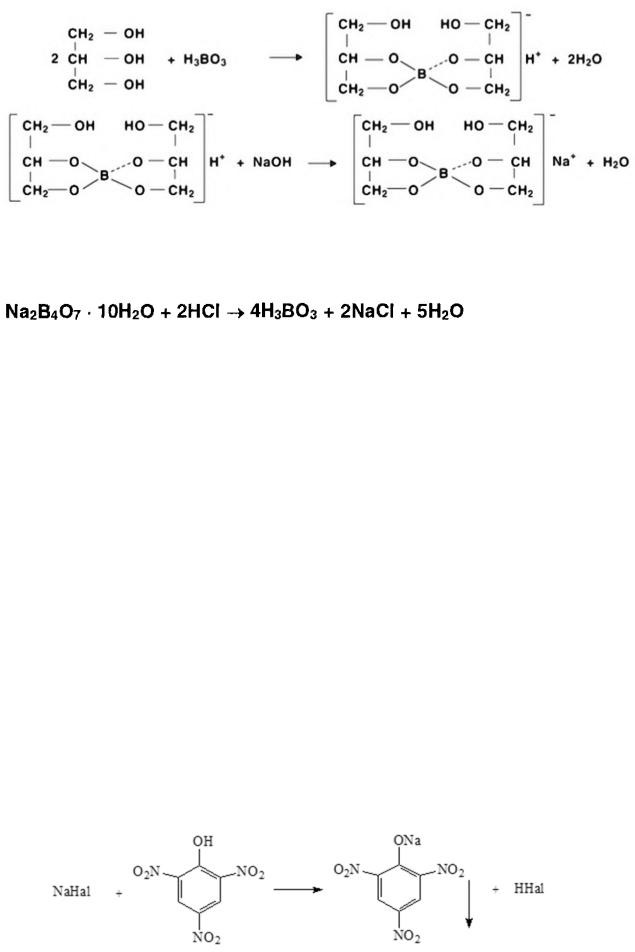
Na2B4O7
Ацидиметрическое титрование. Индикатор метиловый оранжевый
Хранение
В укупоренной таре
Применение
Антисептики
Препарат
натрия гидрокарбонат Natrii hydrocarbonas NaHCO3
лития карбонат Lithii carbonas Li2CO3
Физические свойства
NaHCO3 Белый кристаллический порошок без запаха, растворим в воде Li2CO3 Белый кристаллический порошок, трудно растворим в воде,
Подлинность
Качественные на Na+
1)Желтое пламя
2)С пикриновой кислотой желтый осадок
